NKT細胞標的治療の学術的背景
NKT細胞標的治療の
学術的背景
1.NKT細胞とその活性化物質の発見
NKT細胞は谷口克先生(前千葉大学免疫発生学教室教授)のグループが1986年に発見した免疫細胞です。
発見されてからしばらくの間、その本質的な働きは不明でしたが、1997年にNKT細胞を活性化させる糖脂質(アルファガラクトシルセラミド、略してアルファガラシル)が発見されてから、その機能を解析する研究が進みました。
NKT細胞は様々な免疫細胞を統率すると同時に、自らも病原体やがん細胞を攻撃し、免疫系における「司令官」として機能することが分かりました。また、アルファガラシルを単独で投与するよりも樹状細胞を介して提示する方が、NKT細胞をより強力に活性化できることも判明しました4)。
がん細胞(黄)を攻撃するNKT細胞(青)
NKT細胞とその活性化物質の発見
NKT細胞は谷口克先生(前千葉大学免疫発生学教室教授)のグループが1986年に発見した免疫細胞です。
発見されてからしばらくの間、その本質的な働きは不明でしたが、1997年にNKT細胞を活性化させる糖脂質(アルファガラクトシルセラミド、略してアルファガラシル)が発見されてから、その機能を解析する研究が進みました。
NKT細胞は様々な免疫細胞を統率すると同時に、自らも病原体やがん細胞を攻撃し、免疫系における「司令官」として機能することが分かりました。また、アルファガラシルを単独で投与するよりも樹状細胞を介して提示する方が、NKT細胞をより強力に活性化できることも判明しました4)。
がん細胞(黄)を攻撃するNKT細胞(青)

2.がんに対するNKT細胞の働き
NKT細胞は血液中を循環していますが、がんが出現すると、現場に集積し、様々な免疫細胞を動員することでがん細胞を攻撃します。NKT細胞は「司令官」として機能し、大きく分けて次の6つの働きがあります。
① 樹状細胞を成熟させる
樹状細胞はがんによって未熟化状態になっていて、そのままではキラーT細胞に対してがん攻撃命令(抗原提示)が出せません。
② がんを攻撃する細胞集団を強化し、増やす
様々な免疫細胞(キラーT細胞、NK細胞、マクロファージ)を強化・増殖させ、がんに総攻撃をかけます。
③ がん細胞への直接攻撃
がん細胞に穴をあけ、細胞死を誘導します。
④ がん細胞による免疫抑制を解除
がん細胞は自身を免疫細胞からの攻撃から守るため、免疫細胞を抑制しています。
⑤ がんによる血管新生を抑制
がんは自分の周りに新しく血管を作って養分や酸素を取り込みます。がんが血管を作れないようにすることで、がんを兵糧攻めにします。
⑥ 長期の免疫記憶作用
がんを記憶する幹細胞を生み出し、長期間がんを攻撃できる体制を構築することで、がんの再発を抑制します。
NKT細胞の活性化経路と機能
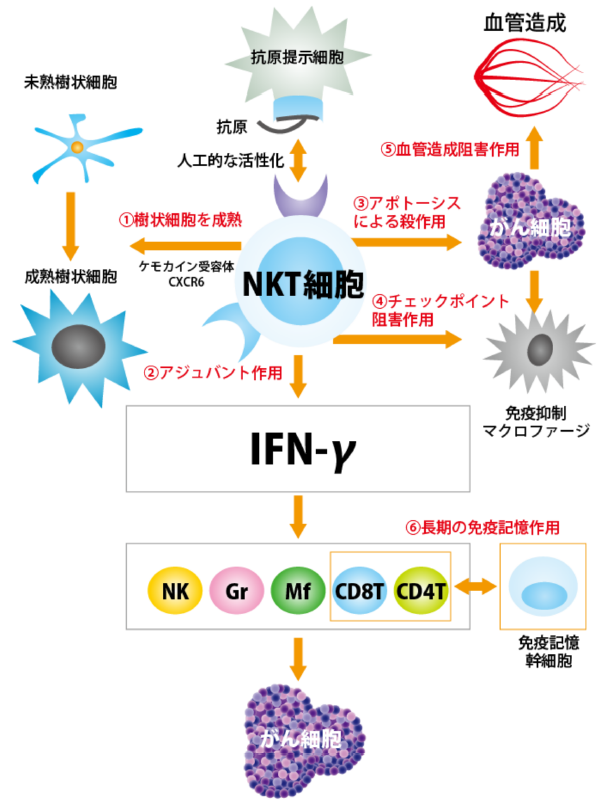
出典:NKT細胞標的がん治療とは がんプラス
がんに対するNKT細胞の働き
NKT細胞は血液中を循環していますが、がんが出現すると、現場に集積し、様々な免疫細胞を動員することでがん細胞を攻撃します。NKT細胞は「司令官」として機能し、大きく分けて次の6つの働きがあります。
① 樹状細胞を成熟させる
樹状細胞はがんによって未熟化状態になっていて、そのままではキラーT細胞に対してがん攻撃命令(抗原提示)が出せません。
② がんを攻撃する細胞集団を強化し、増やす
様々な免疫細胞(キラーT細胞、NK細胞、マクロファージ)を強化・増殖させ、がんに総攻撃をかけます。
③ がん細胞への直接攻撃
がん細胞に穴をあけ、細胞死を誘導します。
④ がん細胞による免疫抑制を解除
がん細胞は自身を免疫細胞からの攻撃から守るため、免疫細胞を抑制しています。
⑤ がんによる血管新生を抑制
がんは自分の周りに新しく血管を作って養分や酸素を取り込みます。がんが血管を作れないようにすることで、がんを兵糧攻めにします。
⑥ 長期の免疫記憶作用
がんを記憶する幹細胞を生み出し、長期間がんを攻撃できる体制を構築することで、がんの再発を抑制します。
NKT細胞の活性化経路と機能

出典:NKT細胞標的がん治療とは がんプラス
3.NKT細胞を標的としたがん治療理論の考案
がんは自己細胞由来なのでNKT細胞を活性化する分子を持っていません。
したがって、NKT細胞をがん治療のために利用するには、人工的に活性化する必要があります。そこで、アルファガラシルを用いてNKT細胞を活性化する「NKT細胞標的がん治療」が考案されました。具体的にはNKT細胞を樹状細胞を介してアルファガラシルで活性化し、アジュバント作用を引き出します。
アジュバントとは、ラテン語の「助ける」という意味をもつ ‘adjuvare’ という言葉を語源に持ち、アジュバント作用とは「がんを攻撃する免疫細胞集団を強化し、増やす」という意味です。「NKT細胞標的治療」の手順は次の通りです。
①患者さんの血液を採取します。
②血液中の樹状細胞を増やし、NKT細胞の活性化物質であるアルファガラシルを取り込ませます。
③アルファガラシルを取り込んだ樹状細胞を点滴で患者さんに戻します。
NKT細胞標的治療のメカニズム
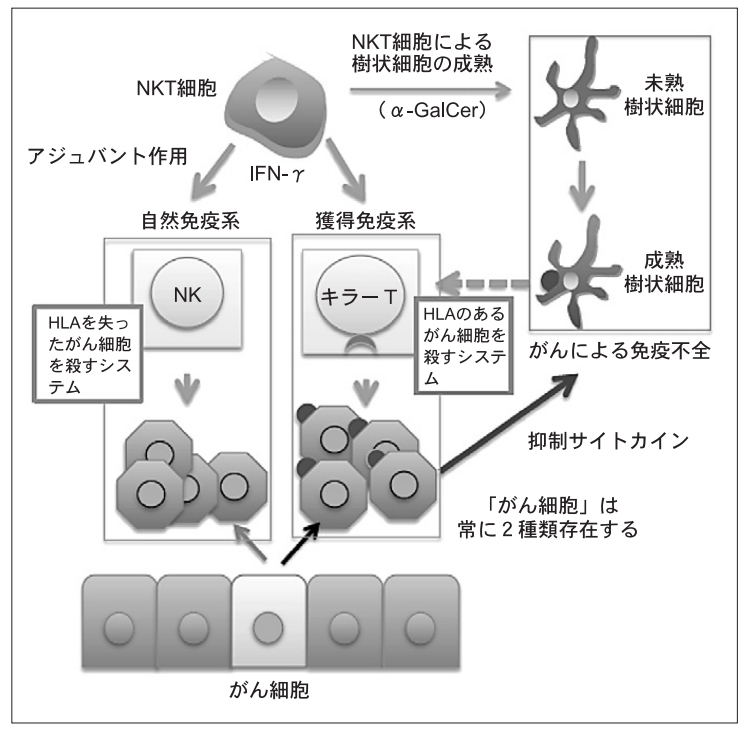
出典:血液フロンティア vol23,No.7, 2013
NKT細胞を標的としたがん治療理論の考案
がんは自己細胞由来なのでNKT細胞を活性化する分子を持っていません。
したがって、NKT細胞をがん治療のために利用するには、人工的に活性化する必要があります。そこで、アルファガラシルを用いてNKT細胞を活性化する「NKT細胞標的がん治療」が考案されました。具体的にはNKT細胞を樹状細胞を介してアルファガラシルで活性化し、アジュバント作用を引き出します。
アジュバントとは、ラテン語の「助ける」という意味をもつ ‘adjuvare’ という言葉を語源に持ち、アジュバント作用とは「がんを攻撃する免疫細胞集団を強化し、増やす」という意味です。「NKT細胞標的治療」の手順は次の通りです。
①患者さんの血液を採取します。
②血液中の樹状細胞を増やし、NKT細胞の活性化物質であるアルファガラシルを取り込ませます。
③アルファガラシルを取り込んだ樹状細胞を点滴で患者さんに戻します。
NKT細胞標的治療のメカニズム

出典:血液フロンティア vol23,No.7, 2013
4.NKT細胞標的治療の前臨床試験
NKT細胞標的治療が理論通りにがんに対して有効であるかどうかを検証するために、マウスで実験を実施しました。
最初に行った実験ではマウス体内のNKT細胞を活性化することでアジュバント効果によりNK細胞及びキラーT細胞が活性化されるか、さらに未熟樹状細胞とNKT細胞が反応して成熟樹状細胞に変化するかを検証しました。
予想通り、キラーT細胞、NK細胞、マクロファージといった様々な免疫細胞が活性化・増殖することが確認されました。次にヒトでの臨床試験の前にがん治療マウスモデルで効果を確認しました。
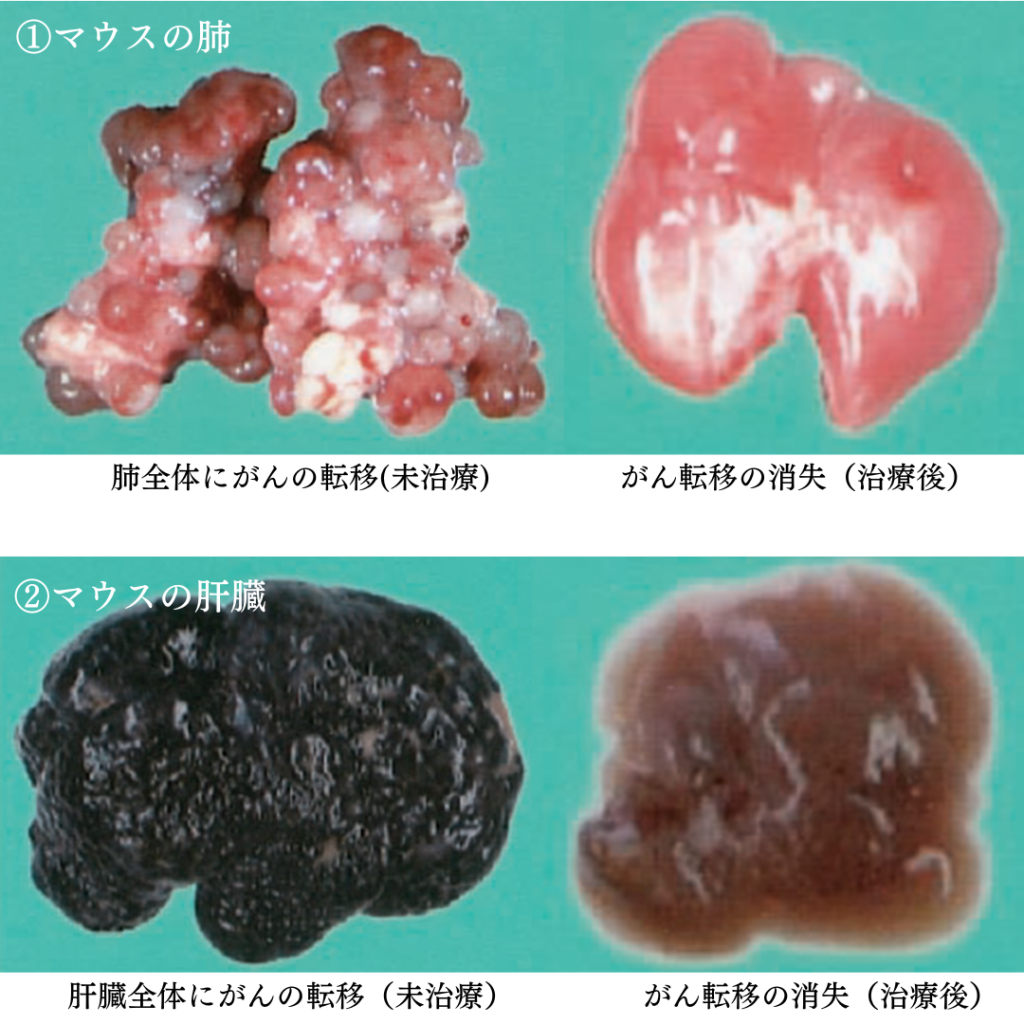
マウスに皮膚がんの一種であるメラノーマを注射すると7日目には肝臓や肺に無数の転移腫瘍が発生します。この状態からアルファガラシルを取り込ませた樹状細胞を静脈投与し、観察すると投与後7日目には肝臓や肺の転移はほぼ消失しました。
これにより、がんが出現した後であっても、NKT細胞標的治療は有効であることが判明しました。
NKT細胞標的治療の前臨床試験
NKT細胞標的治療が理論通りにがんに対して有効であるかどうかを検証するために、マウスで実験を実施しました。
最初に行った実験ではマウス体内のNKT細胞を活性化することでアジュバント効果によりNK細胞及びキラーT細胞が活性化されるか、さらに未熟樹状細胞とNKT細胞が反応して成熟樹状細胞に変化するかを検証しました。
予想通り、キラーT細胞、NK細胞、マクロファージといった様々な免疫細胞が活性化・増殖することが確認されました。次にヒトでの臨床試験の前にがん治療マウスモデルで効果を確認しました。
マウスに皮膚がんの一種であるメラノーマを注射すると7日目には肝臓や肺に無数の転移腫瘍が発生します。この状態からアルファガラシルを取り込ませた樹状細胞を静脈投与し、観察すると投与後7日目には肝臓や肺の転移はほぼ消失しました。
これにより、がんが出現した後であっても、NKT細胞標的治療は有効であることが判明しました。
5.NKT細胞標的治療の臨床試験
千葉大学病院と理化学研究所は共同で進行肺がん患者さん(手術、照射線治療、抗がん剤治療などいずれも不成功であり、予測平均生存期間4.6か月の17名)に対してNKT細胞標的治療の臨床試験を開始しました。
NKT細胞標的治療群全症例の平均生存期間は約20か月と4倍以上延長しました。また、NKT細胞標的がん治療を受けた60%の患者さんは初回の治療だけで、その後は3年間治療を追加せず観察するだけであったにもかかわらず、原発腫瘍の大きさは変わらず、転移もなく、平均生存期間は約30か月と、分子標的治療群のそれと比べても3倍の有意な延長がみられました。
以降、NKT細胞標的がん治療は食道がん、上顎がん、咽頭癌、口腔がんなどの”頭頚部がん”に対しても有効性が確認され、千葉大学病院は国に対して先進医療Bを申請し、承認されました。
NKT細胞標的治療第二相臨床試験
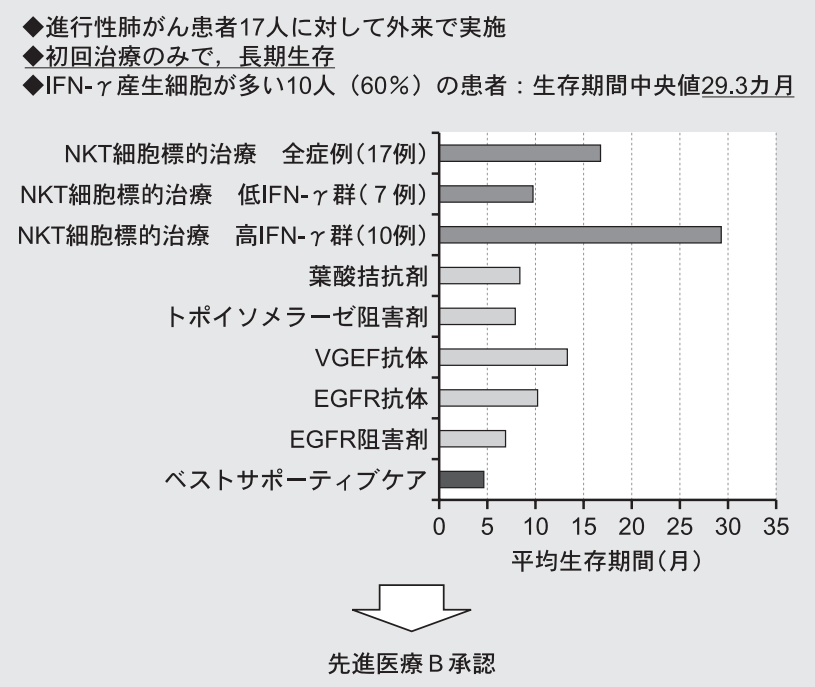
出典:血液フロンティア vol23,No.7, 2013
NKT細胞標的治療の臨床試験
千葉大学病院と理化学研究所は共同で進行肺がん患者さん(手術、照射線治療、抗がん剤治療などいずれも不成功であり、予測平均生存期間4.6か月の17名)に対してNKT細胞標的治療の臨床試験を開始しました。
NKT細胞標的治療群全症例の平均生存期間は約20か月と4倍以上延長しました。また、NKT細胞標的がん治療を受けた60%の患者さんは初回の治療だけで、その後は3年間治療を追加せず観察するだけであったにもかかわらず、原発腫瘍の大きさは変わらず、転移もなく、平均生存期間は約30か月と、分子標的治療群のそれと比べても3倍の有意な延長がみられました。
以降、NKT細胞標的がん治療は食道がん、上顎がん、咽頭癌、口腔がんなどの”頭頚部がん”に対しても有効性が確認され、千葉大学病院は国に対して先進医療Bを申請し、承認されました。
NKT細胞標的治療第二相臨床試験

出典:血液フロンティア vol23,No.7, 2013
NKT細胞の発見から標的がん
治療の開発に至るまでの論文
NKT細胞の発見。1986年に単一のVα14抗原受容体(マウス)をもつユニークなリンパ球として発見され、後にNKT細胞と命名されました。
1997年にNKT細胞が糖脂質アルファガラクトシルセラミドにより活性化されることが発見されました。
1999年にマウスでNKT細胞標的治療の前臨床試験を実施しました。皮膚ガンの一種である悪性黒色腫(メラノーマ)の肝臓への転移を大幅に減らすことが示されました。
2005年に進行肺がん患者さんに対してNKT細胞標的治療の第1相試験が千葉大学医学部で実施されました。重篤な有害事象は認められませんでした。
2006年に進行肺がん患者さんに対して体外活性化NKT細胞移植の第1相臨床試験が千葉大学医学部で実施されました。重篤な有害事象は認められませんでした。
2009年に進行肺がん患者さんに対してNKT細胞標的治療の第2相臨床試験が千葉大学医学部で実施されました。NKT細胞標的治療全症例の平均生存期間は初回治療だけで約20か月(通常生存期間の4倍以上延長)ででした。
2016年にiPS細胞からNKT細胞を誘導することに成功しました。
ご相談・お問合せ
詳しい治療内容や事例、ご不安など、
お気軽にご相談ください。
メールでのお問合わせは
こちらから
お電話でのお問合せは
こちらから
当院はNKT細胞培養の技術提供元である、「株式会社理研免疫再生医学」との提携医療機関です。
お電話には株式会社理研免疫再生医学がお応えいたします。